大株红景天注射液治疗晚期非小细胞肺癌患者的临床效果
周肖龙1 成文娜1 张敬毅2▲
1.滨州医学院附属医院药学部,山东滨州 256601;2.山东省淄博市第一医院药学部,山东淄博 255200
[摘要]目的 探讨大株红景天注射液治疗晚期非小细胞肺癌(NSCLC)患者的临床效果。方法 选取2018年1~12月于滨州医学院附属医院住院的120例晚期NSCLC患者作为研究对象,采用随机数字表法将其分为对照组和治疗组,每组各60例。对照组予以复方苦参注射液及对症治疗,治疗组在此基础上给予大株红景天注射液进行治疗。比较两组患者治疗前后的血清肿瘤标志物水平、中医症状积分及免疫功能指标水平;比较两组患者的近期疗效;比较两组患者治疗前后的生活质量评分。结果 两组患者治疗后的癌胚抗原(CEA)、细胞角蛋白19片段(CYFRA21-1)、糖类抗原19-9(CA19-9)、神经元特异性烯醇化酶(NSE)水平均低于治疗前,差异有统计学意义(P<0.05);治疗组患者治疗后的CEA、CYFRA21-1、CA19-9、NSE均低于对照组,差异有统计学意义(P<0.05)。两组患者治疗后的咳嗽咯痰、胸闷气短、腹胀纳呆、恶心欲吐和四肢无力中医症状积分低于治疗前,差异有统计学意义(P<0.05);治疗组患者治疗后的咳嗽咯痰、胸闷气短、腹胀纳呆、恶心欲吐和四肢无力中医症状积分低于对照组,差异有统计学意义(P<0.05)。治疗组患者的治疗总有效率、稳定率均高于对照组,差异有统计学意义(P<0.05)。治疗后,两组患者的CD4+、CD4+/CD8+高于治疗前,CD8+低于治疗前,差异有统计学意义(P<0.05);治疗组患者治疗后的CD4+、CD4+/CD8+高于对照组,CD8+低于对照组,差异有统计学意义(P<0.05)。治疗组患者治疗后的呼吸困难、食欲减退、咳嗽、咳血、疼痛评分低于对照组,差异有统计学意义(P<0.05)。结论 大株红景天注射液可以缓解晚期NSCLC患者中医证候,提高晚期NSCLC患者的临床治疗效果,提高免疫功能,改善临床症状,值得临床应用。
[关键词]晚期非小细胞肺癌;大株红景天注射液;生活质量;血清肿瘤标志物
肺癌是最常见的恶性肿瘤,其发病率及死亡率正在逐年增加,在癌症病患人群中男性患者居高不下,而且2/3的患者确诊已属晚期,失去了手术机会,其中非小细胞肺癌(NSCLC)占肺癌病例数的70%~80%,放化疗、靶向药物、中医药是晚期NSCLC重要的治疗方法。由于肺癌多属中老年患者,各种生理机能减退,对化疗药物和放射线的耐受性较差,在抑制肿瘤生长的同时,也带来治疗相关毒性的增加,影响到患者的生存质量[1]。红景天的抗肿瘤研究起于20世纪中期,研究证明,不同组分的红景天可以通过调节机体免疫、干扰肿瘤细胞DNA形成、阻滞或抑制癌细胞分裂、诱导分化、诱导凋亡、抑制新生肿瘤血管等方面来对抗肿瘤,是一种安全有效的免疫调节剂[2]。本研究选取于滨州医学院附属医院住院的120例晚期NSCLC患者作为研究对象,探讨大株红景天注射液治疗晚期NSCLC患者的临床效果,观察患者的中医症状、临床针状、血清肿瘤标志物、免疫功能、近期疗效等指标,旨在为更好地发挥中西医结合治疗肺癌提供客观依据,现报道如下。
1 资料与方法
1.1 一般资料
选取2018年1~12月于滨州医学院附属医院住院的120例晚期NSCLC患者作为研究对象,采用随机数字表法将其分为对照组和治疗组,每组各60例。治疗组中,男38例,女22例;平均年龄(68±6)岁;T分期:T1 25例,T2 25例,T3~T4 10例;N分期:N0 34例,N1 3例,N2 23例。对照组中,男39例,女21例;平均年龄(67±7)岁;T分期:T1 24例,T2 25例,T3~T4 11例;N分期:N0 33例,N1 2例,N2 25例。两组患者的性别、年龄、T分期、N分期等一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究已经滨州医学院附属医院医学伦理委员会审核批准,所有患者均签署知情同意书。
1.2 诊断标准
①所有患者均符合《中国原发性肺癌诊疗规范(2015年版)》[3]和《中国晚期原发性肺癌诊治专家共识(2016年版)》[4]诊断标准;②患者均符合中医症候辨证标准[4]。参照国家中医药管理局“十一五”重点专科协作组肺癌诊疗方案,晚期NSCLC符合肺癌气滞血瘀证,本文结合导师临床经验制定气滞血瘀证的判断标准。
1.3 纳入标准
①经X线或CT诊断为原发性肺癌的患者,有可测量病灶,并符合下列条件者均可纳入临床观察病例:经病理学或细胞学证实为原发性肺癌,病理为腺癌、鳞癌、大细胞癌;②中医辨证为气滞血瘀证;③未经其他西医抗肿瘤药物治疗,或放化疗、靶向药物治疗结束2个月以上,肺部仍有病灶者;④肿瘤临床(TNM)分期为Ⅲb、Ⅳ期,无法手术或拒绝接受手术、放化疗者;⑤基因检测无突变者或未检测者;⑦年龄18~70岁;⑧卡氏评分≥60分,预计生存期>3个月者;⑨意识清楚,能顺利回答问题及配合治疗者,患者对治疗方案的依从性较高[4]。
1.4 排除标准
①患有心血管系统、呼吸系统、泌尿系统疾病等的患者和造血系统严重损害者;②治疗过程中患者的身体其他系统出现严重疾病,或患者的病情恶化、病情危急;③因个人原因无法完成整个疗程,或者申请退出者;④依从性较差的患者,不配合跟踪统计者;⑤对本研究中使用药物过敏者,或因药物不耐受而出现严重不良事件患者;⑥精神及神志障碍者,脑转移患者中出现精神意识、失去交流能力者;⑦中医四诊信息不完整者[5];⑦近1个月有明显活动性出血倾向,女性为月经期,应用溶栓、支架等急性抗凝治疗者。
1.5 方法
对照组:将复方苦参注射液(山西振东制药股份有限公司,生产批号:201712-38,规格:5 ml/支)20 ml,加入生理盐水200 ml稀释后静脉滴注,1次/d,50~60滴/min。
治疗组:在对照组的基础上将大株红景天注射液(通化玉圣药业有限公司,生产批号:B0173827,规格:5 ml/支)10 ml加入5%葡萄糖注射液或生理盐水250 ml中静脉滴注,1次/d,50~60滴/min。
两组患者均治疗10 d(1个疗程)。
1.6 观察指标及评价标准
比较两组患者治疗前后的血清肿瘤标志物水平、中医症状积分及免疫功能指标水平;比较两组患者的近期疗效;比较两组患者治疗前后的生活质量评分。
①测定两组患者治疗前后的血清肿瘤标志物水平。应用I2000型化学发光分析仪(美国雅培公司)及其配套试剂,检测患者的血清肿瘤标志物水平,包括癌胚抗原(CEA,批号:52159LF00)、糖类抗原19-9(CA19-9,批号:43073M500)、细胞角蛋白19片段(CYFRA21-1,批号43084M500)、神经元特异性烯醇化酶(NSE,批号:18686701)。②比较两组患者治疗前后的中医症状积分。依据“原发性肺癌症状分级量化表”中的症候评分标准,对两组患者的临床症状进行分级量化评分,按照量表,肺癌主要症状为咳嗽咯痰、胸闷气短、腹胀纳呆、恶心欲吐及四肢无力,每项症状按无、轻、中、重,分别计0、1、2、3分。③免疫功能指标的测定。于治疗前(第0天)清晨及治疗后(第11天)清晨在患者未食用早餐的情况下抽血,应用枸橼酸钠抗凝,采用FC500流式细胞仪(美国贝克曼)测定两组患者的T淋巴细胞亚群指标(包括CD4+、CD8+、CD4+/CD8+)水平。④比较两组患者的近期疗效。临床疗效评价标准,采用2004年循证医学实体瘤的疗效评价标准(RECSIT)[6]考察两组患者的近期疗效。完全缓解(CR):所有目标病灶均消失;部分缓解(PR):基线病灶长径总和缩小≥30%;疾病稳定(SD):基线病灶长径总和有缩小但未达PR,或有增加但未达疾病进展(PD);PD:基线病灶长径总和增加≥20%或出现新病灶。总有效率=(CR+PR)例数/总例数×100%,稳定率=(CR+PR+SD)例数/总例数×100%。⑤比较两组患者治疗前后的临床症状评分。治疗前后,参照肺癌症状量表(LCSS)分别从呼吸困难、食欲减退、咳嗽、咳血及疼痛等方面进行评价。各项目的分值范围均为0~100分,分值越高,表示临床症状越严重,分值越低,表示临床症状越轻微。
1.7 统计学方法
采用SPSS 13.0统计学软件进行数据分析,计量资料用均数±标准差(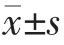 )表示,两组间比较采用t检验;计数资料用率表示,组间比较采用χ2检验,以P<0.05为差异有统计学意义。
)表示,两组间比较采用t检验;计数资料用率表示,组间比较采用χ2检验,以P<0.05为差异有统计学意义。
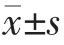 )表示,两组间比较采用t检验;计数资料用率表示,组间比较采用χ2检验,以P<0.05为差异有统计学意义。
)表示,两组间比较采用t检验;计数资料用率表示,组间比较采用χ2检验,以P<0.05为差异有统计学意义。2 结果
2.1 两组患者治疗前后血清肿瘤标志物水平的比较
治疗前,两组患者的血清肿瘤标志物(CEA、CYFRA21-1、CA19-9、NSE)水平比较,差异无统计学意义(P>0.05);治疗后,两组患者的CEA、CYFRA21-1、CA19-9、NSE水平均低于治疗前,差异有统计学意义(P<0.05);治疗组患者治疗后的CEA、CYFRA21-1、CA19-9、NSE水平均低于对照组,差异有统计学意义(P<0.05)(表1)。
表1 两组患者治疗前后血清肿瘤标志物水平的比较

.jpg)
与本组治疗前比较,a P<0.05;与对照组治疗后比较,b P<0.05
2.2 两组患者治疗前后中医症状积分的比较
治疗前,两组患者的咳嗽咯痰、胸闷气短、腹胀纳呆、恶心欲吐和四肢无力中医症状积分比较,差异无统计学意义(P>0.05);治疗后,两组患者的咳嗽咯痰、胸闷气短、腹胀纳呆、恶心欲吐和四肢无力中医症状积分低于治疗前,差异有统计学意义(P<0.05);治疗组患者治疗后的中医症状积分:咳嗽咯痰、胸闷气短、腹胀纳呆、恶心欲吐和四肢无力中医症状积分低于对照组,差异有统计学意义(P<0.05)(表2)。
2.3 两组患者近期疗效的比较
治疗组患者的治疗总有效率、稳定率均高于对照组,差异有统计学意义(P<0.05)(表3)。
2.4 两组患者治疗前后免疫功能指标水平的比较
治疗前,两组患者的T淋巴细胞亚群(CD4+、CD8+、CD4+/CD8+)水平比较,差异无统计学意义(P>0.05);治疗后,两组患者的CD4+、CD4+/CD8+高于治疗前,CD8+低于治疗前,差异有统计学意义(P<0.05);治疗组患者治疗后的CD4+、CD4+/CD8+高于对照组,CD8+低于对照组,差异有统计学意义(P<0.05)(表4)。
表2 两组患者治疗前后中医症状积分的比较(分,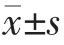 )
)
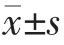 )
).jpg)
与本组治疗前比较,a P<0.05;与对照组治疗后比较,b P<0.05
表3 两组患者近期疗效的比较[n(%)]
.jpg)
表4 两组患者治疗前后免疫功能指标水平的比较(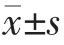 )
)
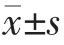 )
).jpg)
与本组治疗前比较,a P<0.05;与对照组治疗后比较,b P<0.05
2.5 两组患者治疗前后临床症状评分的比较
治疗前,两组患者的呼吸困难、食欲减退、咳嗽、咳血、疼痛评分比较,差异无统计学意义(P>0.05)。治疗后,两组患者的呼吸困难、食欲减退、咳嗽、咳血、疼痛评分均低于治疗前,差异有统计学意义(P<0.05);治疗后,治疗组患者的呼吸困难、食欲减退、咳嗽、咳血、疼痛评分均低于对照组,差异有统计学意义(P<0.05)(表5)。
3 讨论
肺癌对人类生命安全的影响巨大,其中NSCLC占肺癌病例数的70%~80%,虽然手术是目前治疗肺癌的主要手段,但是符合手术条件的患者寥寥无几,大多数患者发现时已处于中晚期,已失去手术机会[7]。近年来,癌症的发病率在不断增高,对人类的健康造成了严重危害。随着当今医疗技术的进步和医学模式的改变,治疗癌症时不仅仅是缩小肿瘤,同时也要改善患者的生活质量。影响癌症患者生活质量的因素主要是癌症恶液质,有报道[8]显示,约有80%的中晚期癌症患者会出现恶液质,还会有部分晚期癌症患者因为恶液质致死[9]。对于NSCLC的治疗措施主要分为手术治疗、化疗、局部放疗、靶向治疗、免疫治疗、中医药治疗。近年来中医药治疗NSCLC的研究增多,主要是中医药联合化疗、放疗、靶向治疗方面的研究[10]。
表5 两组患者治疗前后临床症状评分的比较(分, )
)
 )
)
与本组治疗前比较,a P<0.05;与对照组治疗后比较,b P<0.05
祖国医学[11]对肺癌也有文献记载,《难经·论五脏积病》称:“肺之积,名息贲……喘咳,发肺塞。”《济生方》论述:“息贲之状,在右胁下,复大如杯……,喘息奔溢,是为肺积。”肺癌是在内虚的基础上,各种致病因素相互作用,导致以气血功能障碍,引起病理产物聚结而引起的改变。中医学的精髓是辨证施治,目前关于肺癌的分型众说纷纭,临床上多以医家的临证经验划分证型和处方用药[12]。红景天的主要化学成分为黄酮类、糖苷类、有机酸类等,其中红景天苷、酪醇、大花红天素及没食子酸是红景天中的主要有效成分。黄酮类化合物对血管壁有软化作用,可以通过对血流动力学的影响来保护脑血管;其中黄酮及红景天苷主要对脂质成分起作用,这些成分能祛除血液中过多的脂质成分和沉积在血管上的脂质,同时抑制过氧化脂质的生成及血小板的凝集,具有改善微循环及抗氧化应激等作用[13]。红景天是传统中药,具有补气清肺、活血化瘀之功效。大株红景天注射液取自景天科植物花红景天的根茎,是由大株红景天经多道工序提纯制成的中药注射液,主要有效成分是红景天苷,研究发现大株红景天注射液具有辅助治疗肿瘤作用,对肝癌、肺癌、膀胱癌等肿瘤细胞有明显的抑制和杀伤作用,并且大株红景天注射液能改善患者细胞免疫水平,辅助提高化疗药物的抗肿瘤功效,同时表现出降低化疗药物毒性的趋势[14]。
CEA是早期广谱肿瘤的标志物,可以提示肺癌、乳腺癌、胃癌等腺癌类肿瘤,观察到肿瘤患者的CEA血清含量有提示作用[15]。CA19-9是糖类蛋白肿瘤标志物,其血清含量升高可能代表腺瘤的出现,多种腺瘤都可以由血清体现出来。癌与非癌可以由CYFR21-1进行检验。NSE是国际公认的肺癌提示的肿瘤标志物[16]。本研究结果显示,治疗后,两组患者的CEA、CYFRA21-1、CA19-9、NSE水平均低于治疗前,差异有统计学意义(P<0.05);治疗组患者的CEA、CYFRA21-1、CA19-9、NSE水平均低于对照组,差异有统计学意义(P<0.05)。说明大株红景天注射液对癌症有辅助治疗效果,还可以提高患者的细胞免疫水平,增强化疗药物的作用,减轻化疗药物对患者身体的损害。身体免疫力的标志之一是T淋巴细胞亚群含量,肿瘤细胞会降低细胞免疫功能,使得CD8+含量上升,而CD8+的上升会抑制细胞的免疫力,进而导致CD3+、CD4+及CD4+/CD8+比值的下降,身体免疫力的下降,更加使得肿瘤细胞疯狂扩散[17-18]。本研究结果显示,治疗后,两组患者的CD4+、CD4+/CD8+高于治疗前,CD8+低于治疗前,差异有统计学意义(P<0.05);治疗组患者治疗后的CD4+、CD4+/CD8+高于对照组,CD8+低于对照组,差异有统计学意义(P<0.05)。说明大株红景天与复方苦参注射液这两种药品的效果可以修护化疗药物对患者身体的损害,使得患者身体的免疫功能得到保护,两种药品辅助使用可以保护患者的免疫功能减少损伤程度。本研究结果显示,治疗后,两组患者的咳嗽咯痰、胸闷气短、腹胀纳呆、恶心欲吐和四肢无力中医症状积分低于治疗前,差异有统计学意义(P<0.05);治疗组患者治疗后的中医症状积分:咳嗽咯痰、胸闷气短、腹胀纳呆、恶心欲吐和四肢无力中医症状积分低于对照组,差异有统计学意义(P<0.05)。治疗组患者的治疗总有效率、稳定率均高于对照组,差异有统计学意义(P<0.05)。说明大株红景天与复方苦参注射液联合治疗,有助于改善晚期NSCLC患者的临床症状,提高近期疗效。本研究结果显示,治疗后,两组患者的呼吸困难、食欲减退、咳嗽、咳血、疼痛评分均低于治疗前,差异有统计学意义(P<0.05);治疗后,治疗组患者的呼吸困难、食欲减退、咳嗽、咳血、疼痛评分均低于对照组,差异有统计学意义(P<0.05)。说明大株红景天与复方苦参注射液联合治疗,可以改善患者的临床症状,提高患者生活质量,值得临床借鉴参考。
综上所述,大株红景天注射液在治疗晚期NSCLC患者中具有较好的应用效果,对比单独使用复方苦参注射治疗,其具有更高有效率和稳定率,从大株红景天注射液治疗晚期NSCLC患者的作用机制看,其抑制了患者氧自由基的生成,对患者免疫功能的改善有积极帮助,治疗效果良好,且改善患者的临床症状。
[参考文献]
[1]江琳,贾英杰.大株红景天注射液对非小细胞肺癌患者D-二聚体的影响及预后因素分析[J].亚太传统医药,2017,13(12):151-154.
[2]栗莉芳,王海英,闫翠芳,等.大株红景天注射液对非小细胞肺癌患者化疗后生活质量及不良反应的影响[J].临床合理用药杂志,2015,8(19):54-55.
[3]支修益,石远凯,于金明.中国原发性肺癌诊疗规范(2015年版)[J].中华肿瘤杂志,2015,37(1):67-68.
[4]石远凯,孙燕,于金明,等.中国晚期原发性肺癌诊治专家共识(2016年版)[J].中国肺癌杂志,2016,19(1):7-21.
[5]栗莉芳,王海英,闫翠芳,等.大株红景天注射液对非小细胞肺癌患者免疫功能的影响[J].临床合理用药杂志,2015,8(25):30-31.
[6]高佩.肺复康方联合埃克替尼治疗气阴两虚痰瘀毒结型中晚期非小细胞肺癌临床研究[D].长沙:湖南中医药大学,2016:17-18.
[7]张素芳,郝爱芹,王建正.化疗联合参麦注射液对晚期非小细胞肺癌患者细胞免疫及肿瘤恶性程度的影响[J].世界中医药,2017,12(5):136-140,144.
[8]程小峰.大株红景天注射液应用于肺癌化疗患者的临床研究[D].福州:福建中医药大学,2013:11-12.
[9]罗湘玉,杜春玲,黄平,等.大株红景天注射液防治周围型肺癌肺叶切除术后疲劳综合征的临床研究[J].中国医药导报,2016,13(26):144-147.
[10]和殿峰,蒋立峰.益肺消积方对晚期非小细胞肺癌患者血清肿瘤标志物及生活质量的影响[J].中医学报,2017,32(9):1583-1585.
[11]史博文,岳东升,孙冰生,等.治疗前血浆纤维蛋白原及D-二聚体水平联合预测晚期非小细胞肺癌患者预后[J].天津医药,2017,45(4):46-50.
[12]李发祥.阿帕替尼联合GP方案治疗晚期非小细胞肺癌的疗效及安全性[J].实用癌症杂志,2019,34(6):952-955.
[13]何小鹤.化瘀解毒法联合化疗治疗痰瘀互结型中晚期非小细胞肺癌的临床观察[D].郑州:河南中医药大学,2018:9-10.
[14]孙亚华,徐红双,张延勇,等.自拟参麦养心汤联合磷酸肌酸对接受CAF化疗方案的乳腺癌患者氧自由基及心脏功能的影响[J].现代中西医结合杂志,2017,26(23):2528-2531.
[15]胡楠,刘琳,曾媛,等.血清癌胚抗原与肺癌关系的研究进展[J].癌症进展,2020,18(6):547-548,602.
[16]冯白昌.CYFRA21-1、NSE、CEA、CA125、CA19-9联合检测对肺癌的诊断意义[J].中国保健营养,2020,30(10):81.
[17]杨广山,陶宋词,徐媛媛.益气养阴解毒方联合化疗治疗中晚期非小细胞肺癌22例[J].安徽中医药大学学报,2016,35(4):25-27.
[18]邱芝琳,葛信国.益气养阴解毒方联合化疗治疗非小细胞肺癌临床研究[J].中医学报,2014,29(10):1397-1399.
Clinical effect of Sofren Injection in the treatment of patients with advanced non-small cell lung cancer
ZHOU Xiao-long1 CHENG Wen-na1 ZHANGJing-yi2▲
1.Department of Pharmacy,Binzhou Medical University Hospital,Shandong Province,Binzhou 256601,China;2.Department of Pharmacy,the First Hospital of Zibo City,Shandong Province,Zibo 255200,China
1.Department of Pharmacy,Binzhou Medical University Hospital,Shandong Province,Binzhou 256601,China;2.Department of Pharmacy,the First Hospital of Zibo City,Shandong Province,Zibo 255200,China
[Abstract]Objective To explore the clinical effect of Sofren Injection in the treatment of patients with advanced nonsmall cell lung cancer(NSCLC).Methods A total of 120 patients with advanced NSCLC admitted to the Binzhou Medical University Hospital from January to December 2018 were selected as study subjects,and were divided into the control group and the treatment group by the random number table method,with 60 patients in each group.All patients were divided into control group and treatment group by the random number table method,with 60 patients in each group.The control group was given Compound Sophora Flavescens Injection and symptomatic treatment,and the treatment group was given Sofren Injection on this basis.The levels of serum tumor markers,traditional Chinese medicine symptom scores and immune function indexes before and after treatment were compared between the two groups.The short-term efficacy was compared between the two groups.Quality of life scores before and after treatment were compared between the two groups.Results The levels of carcinoembryonic antigen (CEA),cytokeratin 19 fragment(CYFRA21-1),carbohydrate antigen 19-9(CA19-9),and neuron-specific enolase(NSE)in the two groups were lower than those before treatment,with statistically significant differences (P<0.05).After treatment,CEA,CYFRA21-1,CA19-9 and NSE in the treatment group were all lower than those in the control group,with statistically significant differences (P<0.05).The scores of traditional Chinese medicine symptoms of cough and expectoration of sputum,chest congestion and shortness of breath,abdominal distension and stupor,nausea and vomiting,and limb weakness in the two groups after treatment were lower than those before treatment,and the differences were statistically significant(P<0.05).The scores of traditional Chinese medicine symptoms of cough and expectoration of sputum,chest congestion and shortness of breath,abdominal distension and stupor,nausea and vomiting,and limb weakness in the treatment group were lower than those in the control group,with statistically significant differences(P<0.05).The total effective rate and stability of the treatment group were higher than those of the control group,and the differences were statistically significant(P<0.05).The total effective rate and stability of the treatment group were higher than those of the control group,and the difference was statistically significant(P<0.05).After treatment,CD4+and CD4+/CD8+in the two groups were higher than those before treatment,and CD8+was lower than that before treatment,with statistically significant differences (P<0.05).After treatment,CD4+and CD4+/CD8+in the treatment group were higher than those in the control group,and CD8+was lower than that in the control group,with statistically significant differences(P<0.05).The scores of dyspnea,anorexia,cough,hemoptysis and pain in the treatment group were lower than those in the control group,and the differences were statistically significant(P<0.05).Conclusion Sofren Injection can significantly alleviate traditional Chinese medicine symptoms of patients with advanced NSCLC,and significantly improve the clinical treatment effect of patients with intermediate and advanced lung cancer,it can improve the immune function,and improve the clinical symptoms.It is worthy of clinical application.
[Key words]Advanced non-small cell lung cancer;Sofren Injection;Quality of life;Serum tumor markers
[中图分类号]R934.2
[文献标识码]A
[文章编号]1674-4721(2020)8(c)-0017-06
▲通讯作者
(收稿日期:2020-03-31)